Emberi bőrsejtekből állítottak elő petesejteket
A tudomány újabb határát lépte át: sikerült emberi bőrsejtekből teljes értékű, laboratóriumban megtermékenyíthető petesejtet előállítani.A portlandi Oregon Health and Science University (OHSU) kutatói által végzett vizsgálat bizonyítja, hogy a bőrsejtek átprogramozhatók, és az így létrehozott petesejtek fejlődése laboratóriumi körülmények között is elindítható.
Miért jelentős ez a felfedezés?

Világszerte milliók küzdenek meddőséggel, amely gyakran a petesejtek vagy a spermiumok hiányából ered. A mesterséges megtermékenyítés sok páron segít, ám életképes petesejt nélkül nem lehetséges a genetikai kapcsolatú gyermek nemzése. Az OHSU kutatói most olyan bőrsejtekből előállított petesejteket sikeresen megtermékenyítettek, amelyek napokon keresztül fejlődtek, és az eredmények a Nature Communications folyóiratban jelentek meg.
Hogyan működik a módszer?
A kutatók azt a hipotézist tesztelték, hogy egy személy „más sejtjei” átprogramozhatók petesejtekké vagy spermiumokká az in vitro gametogenesis (IVG) eljárással. Egyszerűbben fogalmazva: szinte bármely testsejt átalakítható ivarsejtté, amely aztán laboratóriumban megtermékenyíthető.
Korábbi vizsgálatok már kimutatták, hogy egerek bőrsejtjeivel működik az IVG. Az új tanulmány elsőként igazolta, hogy ez emberi sejtek esetén is lehetséges.
Kihívások a petesejt előállításában
A kutatás során a petesejt magját egy bőrsejt magjával helyettesítették. Azonban az egészséges ivarsejtek egy kromoszómakészletet tartalmaznak, míg a test más sejtjei kettőt. Ha ezt nem korrigálják, az embrió túl sok kromoszómával jönne létre.
A probléma megoldására a tudósok a mitomeiózis nevű eljárást alkalmazták, amely a természetes meiózis folyamatát utánozza, és eltávolítja a felesleges kromoszómákat.
Szomatikus sejtmag-átültetés: SCNT
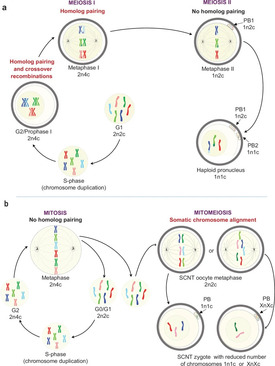
A szomatikus sejtmag-átültetés (SCNT) lehetővé teszi, hogy a szomatikus sejtek közvetlenül funkcionáló oocitákká alakuljanak, bár diploid genommal. A ploiditás csökkentésének érdekében a kutatók a mitomeiózist, egy kísérleti reduktív sejtosztódási folyamatot alkalmazták. Ebben a folyamatban a nem replikálódott (2n2c) szomatikus genomokat enukleált emberi oociták metafázisos citoplazmájába ültetik, ahol idő előtt osztódásra kényszerülnek.
A spermiummal történő megtermékenyítés során azonban az SCNT oociták a metafázisos stádiumban megálltak, jelezve az aktivációs kudarcot. Egy szelektív ciklinfüggő kináz inhibitorral végzett mesterséges aktiválás azonban sikeresen áthidalta ezt a leállást, és biztosította a szomatikus kromoszómák pronukleuszba és poláris testbe történő szegregációját.
In vitro gametogenezis (IVG) és terápiás lehetőségek
A meddőség egyik fő oka, különösen a nők esetében, a petesejtek életkorral összefüggő minőség- és mennyiségcsökkenése, ami gyakran már harmincas évek közepén jelentkezik. Az IVG koncepciója az, hogy a beteg szomatikus sejtjeit indukált pluripotens őssejtekké (iPSC) programozzák, majd funkcionáló ivarsejtekké alakítják.
Egérmodellekben a női IVG működőképességét már bizonyították, ám az emberi csírasejt-fejlődés jelentős különbségei miatt a módszer embereknél még nem alkalmazható. A funkcionális oocitákhoz anyai citoplazmatikus faktorokra, megfelelő meiotikus rekombinációra, kromoszóma-ploiditás csökkentésre és imprint-újraprogramozásra van szükség, hogy a jövőben klinikai alkalmazásokhoz alkalmasak legyenek.
Eredmények és perspektívák
A kutatás során összesen 82 petesejtet hoztak létre, amelyek 9%-a sikeresen megtermékenyült spermium segítségével, majd blasztocitává fejlődött – a kutatók jellemzően az embriók ötödik napjáig vizsgálják azokat.
Bár a módszer még nem alkalmazható klinikai környezetben, és további vizsgálatok szükségesek, a felfedezés rendkívül ígéretes. Ha a kutatók tovább dolgoznak rajta, egy napon új lehetőséget kínálhat a meddőség kezelésére.

